¶ Vom Pilz zur Sequenz
Die DNA-Sequenzierung ist ein mehrstufiger Prozess, der am besten auf mehrere Tage verteilt wird.
Im Schnitt kann jeder Teilschritt an einem Nachmittag durchgeführt werden.
Frei nach Alan Rockefeller:
"Pilze sequenzieren ist schwieriger, als ein Ei zu kochen, aber leichter, als ein Brot zu backen"
Im Internet gibt es zahlreiche Anleitungen, Dokumenationen und Protokolle, die den Prozess beschreiben.
Ähnlich ein Rezept beim Backen, beschreiben Protokolle den Ablauf eines Arbeitsschrittes.
Zur Durchführung des Protokolls sind wenige bis keine Vorkenntnisse über die molekularen Abläufe notwendig, sogleich sie trotzdem sehr hilfreich sein können.
Um einen Kuchen zu backen, muss ich nicht wissen, wie sich die Hitze des Ofens auf die Denaturierung
¶ Welche Pilze können am besten sequenziert werden?
Basidiomyceten, frische und getrocknete Lamellenpilze, Gallertpilze, weichere Porlinge, Myzel, weiche und harte Ascomyceten/Pyrenomyceten.
¶ Welche Sequenzierungsmethode ist die richtige?
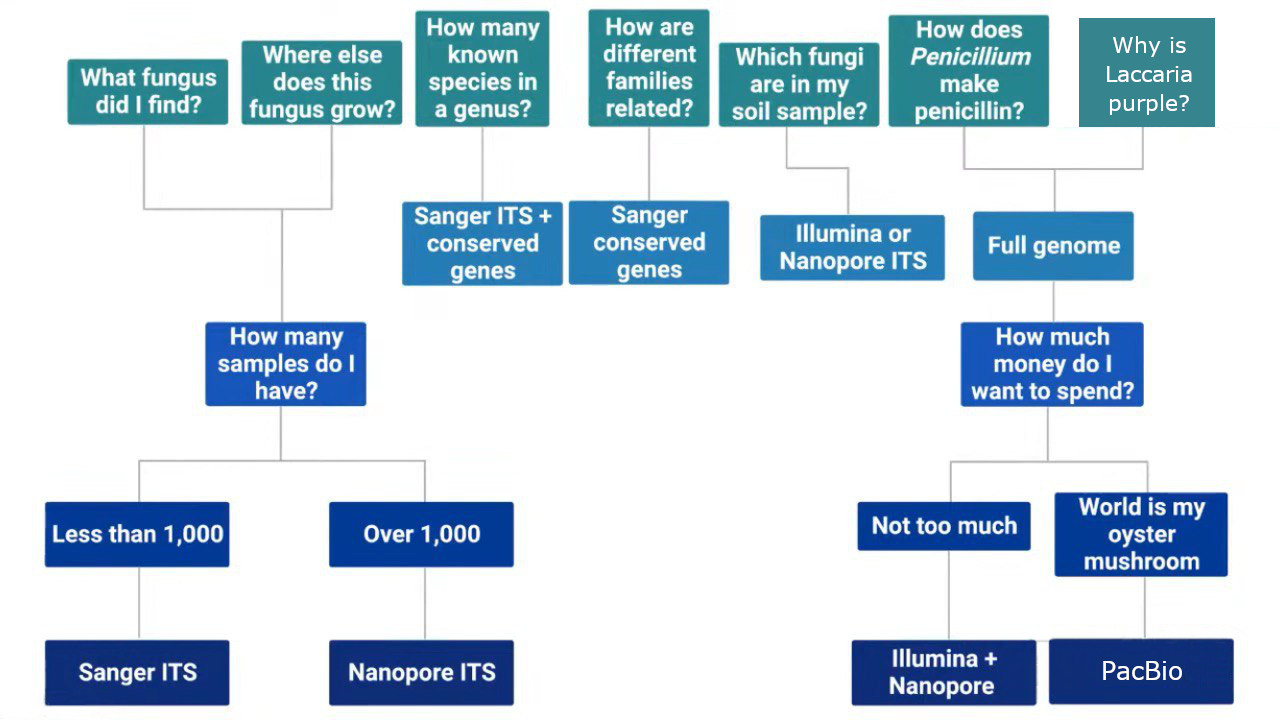
Quelle: Central Texas Mycological Society
Die Methode der Sequenzierung ist abhängig von der Fragestellung.
Im CCL interessieren uns primär die Fragen:
Um welche Pilzart handelt es sich?
Wo auf der Welt wurde die selbe Sequenz dokumentiert?
Sanger Sequenzierung:
Aus Gründen der Praktikabilität und Kosten, wird sich im CCL vor allen Dingen auf die Herstellung von PCR Produkten der jeweiligen Proben konzentriert. Sind die Amplifikate von guter Qualität, werden sie per Post zu Herrn Pablo Alvarado nach Spanien versendet, und dort nach Sanger sequenziert. Diese Sequenzierungsmethode wurde in den 70er Jahren entwickelt und ist allgemein auch als next generation sequencing bekannt.
Nanopore:
Als third generation sequencing werden weiter fortgeschrittene moderne Methoden der Sequenzierung bezeichnet.
Ein Beispiel dafür ist das Nanopore-Verfahren. Die Nanoporen sind eingelassen in eine künstliche Membran, die einen besonders hohen elektrischen Widerstand aufweist. DNA-Moleküle, die die Pore passieren, führen zu einer Verringerung des Stromes. Diese Stromabnahme hat eine für jedes Nukleotid spezifische Amplitude, welche gemessen und dem entsprechenden Nukleotid zugeordnet werden kann. Somit kann die Sequenz sehr genau ermittelt werden. Zudem kommt der Vorteil, dass auf die Amplifikation mittels PCR verzichtet werden kann. Dadurch ist Nanopore sehr relevant für die Sequenzierung von Umwelt-DNA (eDNA). Hierbei werden viele kleine DNA-Moleküle gleichzeitig sequenziert.
Die Nanopore-Technologie ist besonders geeignet für sehr lange Sequenzen bis zu 2 Megabasen (full genome). Dadurch können potentiell auch phylogenetische Untersuchungen vorgenommen, und somit neue Arten beschrieben werden. Im Durchschnitt beträgt die Länge der Fragmente 10er bis in die 100er Kilobasen.
Das Gerät MinIon wird mit sogenannten flowcells (Verbrauchsmaterial) bestückt. 1 Flongle (flowcell mit den Nanoporen) kann eine Anzahl von Basenpaaren sequenzieren, die den fungalen ITS-Regionen von bis zu 960 Pilzexemplaren entspricht. Hierfür müssen die Amplifikate der einzelnen Proben mit Barcodes versehen werden, um sie nach der Nanopore-Sequenzierung bioinformatisch zuordnen zu können. Diese Methode können wir im CCL durchführen, da das Gerät MinIon im Vereinsbesitz ist.
Sobald die Abläufe für die Amplifikationen etabliert sind, widmen wir uns der Inbetriebnahme des Nanopore MinIons.
Wir sind Dankbar für die Unterstützung durch erfahrene und/oder interessierte Personen
Kontakt
folgende Informationen sind frei aus Sigrids PCR Protokoll entnommen.
letztes Update erfolgte am 22. Oktober 2024
¶ Vorbereitung
- Entscheide, welche Pilze verarbeitet werden sollen.
- Trage die Pilze in ein Logbuch/eine Tabelle ein, um den Überblick zu behalten.
- (Falls X-Amp nicht verwendet wird) Verdünne die NaOH-Lösung (1:50 aus Granulat) und den TBE-Puffer (1:10 aus der Stammlösung) – dies muss nur gelegentlich gemacht werden, da die hergestellte Menge für viele Sitzungen ausreicht.
- Zentrifuge vorbereiten.
- Thermocycler einrichten. Falls ein miniPCR-Thermocycler verwendet wird, verbinde ihn mit dem Computer per Kabel oder lade die miniPCR-App herunter und verbinde ihn per Bluetooth. Erstelle Programme für die Amplifikation und den 10-minütigen Hitzeblock (dies muss nur einmal eingerichtet werden) – weitere Anweisungen dazu folgen später.
- Arbeitsbereich reinigen.
- Pilze in der Reihenfolge der Tabelle auf einer Platte auslegen (ich ordne sie nach iNat-Nummer).
- Handschuhe anziehen oder Hände mit Isopropanol reinigen.
- Ein kleines Glas oder eine Sprühflasche mit Isopropanol bereithalten, um die Hände regelmäßig zu desinfizieren.
- Röhrchenstreifen beschriften (für acht Proben werden zwei Streifen mit je acht Röhrchen benötigt).
¶ Extraktion
Methode mit NaOH:
Aus Sigrids Protokoll:
- 30 µl 0,5M NaOH in jedes Tube geben (Pipettenspitzen müssen nicht zwischen den Proben gewechselt werden, solange sie das Pilzgewebe nicht berühren).
- Mit einer Pinzette ein kleines Stück Gewebe vom Pilz abreißen (je kleiner, desto besser, idealerweise so groß wie ein Sesamsamen) und in ein 0,2-ml-Tube geben. Falls das Exemplar nicht sauber ist, aufbrechen und Gewebe aus dem Inneren entnehmen.
- Pinzette zwischen den Proben desinfizieren, indem sie mit einem mit Isopropanol getränkten Papiertuch abgewischt wird.
- Jede Probe für einige Sekunden mit einer Pipettenspitze zerquetschen und zerkleinern – für jede Probe eine frische Spitze verwenden!
- 10 Minuten stehen lassen (in der Zwischenzeit aufräumen).
- 150 µl des verdünnten Tris-8,0-pH-Puffers in jedes Röhrchen geben (Pipettenspitzen müssen nicht zwischen den Proben gewechselt werden, solange sie die Flüssigkeit in den Röhrchen nicht berühren).
- Röhrchenstreifen für 10 Minuten bei 95 °C im Thermocycler erhitzen (sogenannter „Hitzeblock“).
- 5 Minuten lang bei 5.000 U/min oder höher zentrifugieren.
Darauf achten, dass die Zentrifuge ausbalanciert ist, d. h. die gleiche Anzahl von Proben auf jeder Seite zentriert liegt.
- Falls acht Proben verarbeitet werden, den Röhrchenstreifen in zwei Hälften teilen.
- Sicherstellen, dass die Röhrchendeckel richtig verschlossen sind!
Aus Alan Rockefellers Wiki:
¶ Amplifikation (für 25 μL PCR Ansätze)
Kombiniere in einem freien 0,2 ml Röhrchen die folgenden Reagenzien, ausreichend für acht Proben. Führe diesen Schritt zügig durch, da die Reagenzien sofort miteinander reagieren, sobald sie gemischt werden. Die Mischung sollte schnell in den Thermocycler gebracht werden.
¶ Theoretische Mengen für eine PCR Reaktion (25 µL)
12,5 µL Mastermix
1 µL Forward-Primer (ITS1-F)
1 µL Reverse-Primer (ITS4-B)
1(-2) µL Template DNA (DNA-Extraktion der Probe)
9,5 µL destilliertes oder molekulargradiges Wasser
¶ Reale Pipettiermengen, um Verluste auszugleichen (26 µL)
13 µL Mastermix
1 µL Forward-Primer (ITS1-F)
1 µL Reverse-Primer (ITS4-B)
1(-2) µL Template DNA (DNA-Extraktion der Probe)
10 µL destilliertes oder molekulargradiges Wasser
¶ gepoolte Mengen für 8 PCR Reaktionen (26 µL)
- Gesamtvolumen aller Reaktionen: 208 µL
104 µL Mastermix DreamTaq (2X)
8 µL Forward-Primer (ITS1-F)
8 µL Reverse-Primer (ITS4-B)
8 µL Template DNA (DNA-Extraktion der Probe)
Summe: 128 µL
Rest:
80 µL destilliertes oder molekulargradiges Wasser
Mische die Lösung, indem du sie mit der Pipettenspitze aufziehst und wieder herauslässt, sobald du das Wasser hinzugefügt hast.
Pipettiere 26 µL der Mischung in jedes Röhrchen eines Röhrchenstreifens, um Verluste auszugleichen.
Füge jedem dieser Röhrchen 1 µl der Pilzlösung hinzu, die du im Extraktionsschritt vorbereitet hast. Verwende für jede Probe eine neue Pipettenspitze. Da die Menge sehr gering ist, überprüfe visuell, ob du tatsächlich Flüssigkeit aufgenommen hast.
Pipettiere die Mischung ein paar Mal auf und ab, um sie zu vermengen. Verschließe die Röhrchen und schnippe leicht gegen jedes Röhrchen, um sicherzustellen, dass alles gut durchmischt ist.
Setze die Röhrchen in den Thermocycler ein.
Aktualisierte Laufzeiten gemäß dem aktualisierten Alan Rockefeller/CounterCulture Lab-Protokoll:
Falls der Thermocycler noch nicht programmiert wurde, richte das Programm jetzt ein:
Initiale Denaturierung: 2 Minuten bei 95 °C
30 Zyklen mit den folgenden Schritten:
Denaturierung: 30 Sekunden bei 95 °C
Annealing (Anlagerung): 30 Sekunden bei 54 °C für reguläres ITS1, 52 °C für ITS1-KYO2
Verlängerung: 55 Sekunden bei 72 °C
Finale Verlängerung: 120 Sekunden bei 72 °C
Lass das Programm laufen, bis es abgeschlossen ist. Die Proben können anschließend bei Raumtemperatur aufbewahrt werden.
Aus Studie [4]:
PCR was conducted using the buffer system of Ampdirect Plus (Shimadzu) with BIOTAQ HS DNA Polymerase (Bioline) under a temperature profile of
- 95°C for 10 min
followed by 35 cycles at- 94°C for 20 s
- 47°C for 30 s
- 72°C for 20 s (40 s for the entire ITS region)
followed by 72°C for 7 minThe concentration of MgCl2, dNTPs, PCR primers and the template DNA in the reaction buffer were 1,5 mM, 200 µM, 0,5 µM and 1 ng/µl, respectively.
¶ Gel Elektrophorese
¶ Primer Info
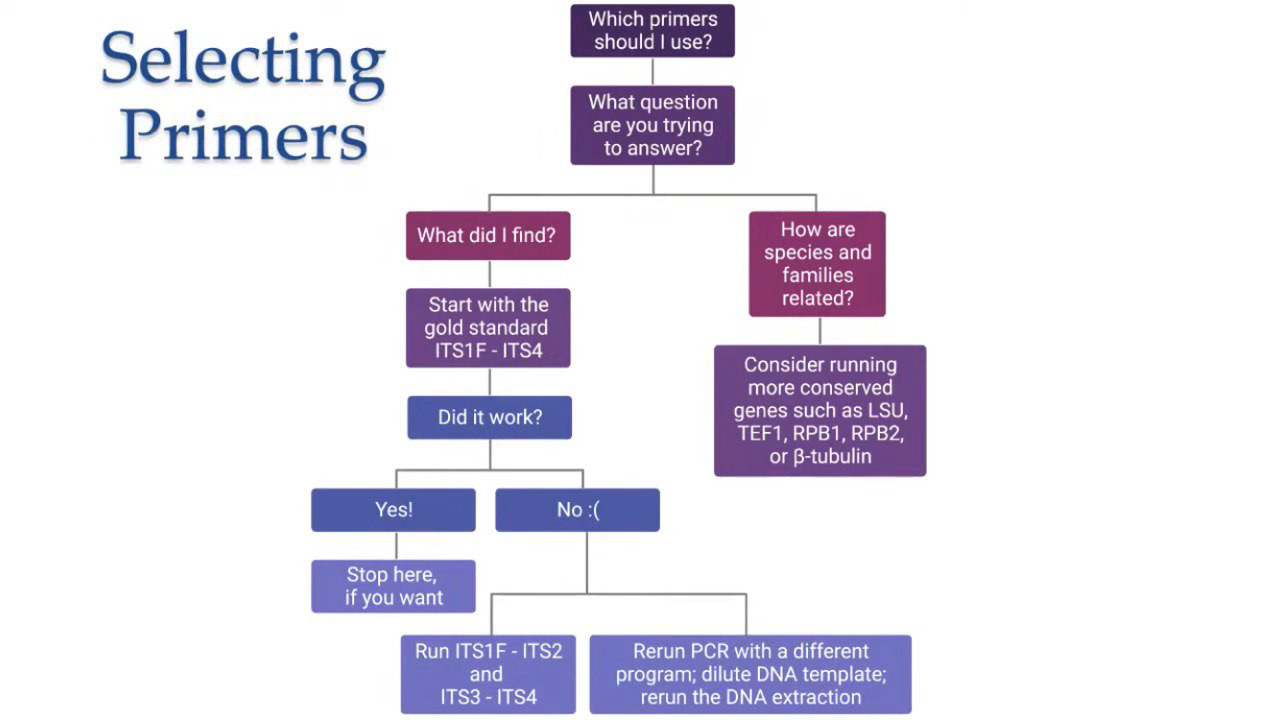
Quelle: Central Texas Mycological Society
¶ Standard Primer
ITS1-F (CTTGGTCATTTAGAGGAAGTAA) (forward Standard, selektiv für fungal)
ITS4-B (CAGGAGACTTGTACACGGTCCAG) (reverse für Basidiomyceten)
ITS4 (TCCTCCGCTTATTGATATGC) (reverse für Ascomyceten)
Vorgehen herkömmlich:
- erstmal ITS1-F / ITS4, falls kein Erfolg
dann- ITS1-F / ITS2 + ITS3 / ITS4
¶ Primer Map (ITS)

Quelle: Central Texas Mycological Society
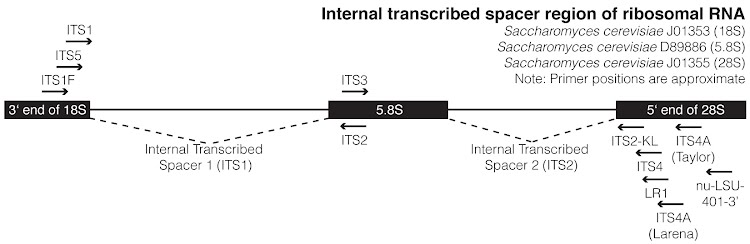
Quelle: Matthew P Nelsen Primer Maps
Tabelle 1 (ITS):
| Primer | F/R | Locus | Position | Sequence | Reference |
|---|---|---|---|---|---|
| *ITS1F | F | 18S | 1731-1752 | CTTGGTCATTTAGAGGAAGTAA | Gardes & Bruns (1993) |
| ITS5 | F | 18S | 1745-1766 | GGAAGTAAAAGTCGTAACAAGG | White et al. (1990) |
| ITS1 | F | 18S | 1769-1787 | TCCGTAGGTGAACCTGCGG | White et al. (1990) |
| ITS3 | F | 5.8S | 31-50 | GCATCGATGAAGAACGCAGC | White et al. (1990) |
| ITS2 | R | 5.8S | 31-50 | GCTGCGTTCTTCATCGATGC | White et al. (1990) |
| *ITS2-KL | R | 28S | 25-44 | TGCTTAAGTTCAGCGGGTA | Lohtander et al. (1998) |
| ITS4 | R | 28S | 41-60 | TCCTCCGCTTATTGATATGC | White et al. (1990) |
| LR1 | R | 28S | 57-73 | GGTTGGTTTCTTTTCCT | Vilgalys & Hester (1990) |
| *ITS4A (Larena) | R | 28S | 71-93 | CGCCGTTACTGGGGCAATCCCTG | Larena et al. (1999) |
| *ITS4A (Taylor) | R | 28S | 96-116 | ATTTGAGCTGTTGCCGCTTCA | D.L. Taylor in Kroken & Taylor (2001) |
| *nu-LSU-136-3’ | R | 28S | 136-154 | CAAATTACAACTCGGACCC | Döring et al. (2000) |
*Primer preferentially amplifies fungi.
Quelle: https://mpnelsen.com/primer-maps-2/
¶ Primer Map (LSU)
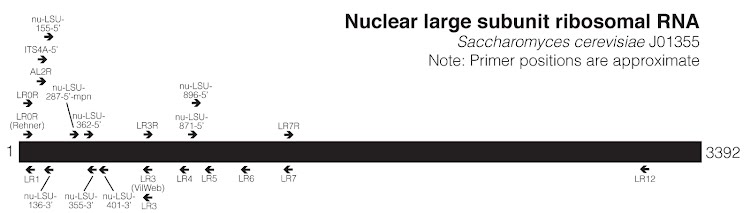
Tabelle 2 (LSU):
| Primer | F/R | Position | Sequence | Reference |
|---|---|---|---|---|
| LR0R (Rehner) | F | 24-42 | GTACCCGCTGAACTTAAGC | Rehner & Samuels (1994) |
| LR0R | F | 26-42 | ACCCGCTGAACTTAAGC | Vilgalys Website? or Cubeta et al. (1991)? |
| LR1 | R | 57-73 | GGTTGGTTTCTTTTCCT | Vilgalys & Hester (1990) |
| AL2R | F | 91-112 | GCGAGTGAAGCGGCAACAGCTC | Mangold et al. (2008) |
| ITS4A-5′ | F | 96-116 | TGAAGCGGCAACAGCTCAAAT | Nelsen et al. (2011)/D.L. Taylor in Kroken & Taylor (2001) |
| nu-LSU-155-5′ | F | 136-155 | GGGTCCGAGTTGTAATTTGT | Döring et al. (2000) |
| nu-LSU-136-3′ | R | 136-154 | CAAATTACAACTCGGACCC | Döring et al. (2000) |
| nu-LSU-287-5′-mpn | F | 270-287 | CGAGTTGTTTGGGAATGC | Nelsen et al. (2011) |
| nu-LSU-362-5′ | F | 344-362 | GCGCACAAGTAGAGTGATC | Döring et al. (2000) |
| nu-LSU-355-3′ | R | 355-376 | GCTTTTCATCTTTCGATCACTC | Döring et al. (2000) |
| nu-LSU-401-3′ | R | 401-419 | CCTTTCAACAATTTCACGT | Döring et al. (2000) |
| LR3 (VilWeb) | R | 635-651 | CCGTGTTTCAAGACGGG | Vilgalys Website |
| LR3 | R | 638-654 | GGTCCGTGTTTCAAGAC | Vilgalys & Hester (1990) |
| LR3R | F | 638-654 | GTCTTGAAACACGGACC | Vilgalys Website? |
| LR4 | R | 838-854 | ACCAGAGTTTCCTCTGG | Vilgalys Website? |
| nu-LSU-871-5′ | F | 854-871 | TGGAGGCTCGCAGCGGTT | Döring et al. (2000) |
| nu-LSU-896-5′ | F | 878-896 | TGCAAATCGATCGTCAAAT | Döring et al. (2000) |
| LR5 | R | 949-965 | ATCCTGAGGGAAACTTC | Vilgalys & Hester (1990) |
| LR6 | R | 1125-1141 | CGCCAGTTCTGCTTACC | Vilgalys & Hester (1990) |
| LR7 | R | 1432-1448 | TACTACCACCAAGATCT | Vilgalys & Hester (1990) |
| LR7-R | F | 1432-1448 | AGATCTTGGTGGTAGTA | Vilgalys & Hester (1990) |
| LR12 | R | 3106-3122 | GACTTAGAGGCGTTCAG | Vilgalys & Hester (1990) |
Quelle: https://mpnelsen.com/primer-maps-2/
¶ Kyoto Primer
ITS_KYO Primer: (annealing bei 47°C)
- erstmal ITS1-F_KYO2 / ITS4, falls kein Erfolg
dann- ITS1-F_KYO2 / ITS2_KYO2 + ITS3_KYO2 / ITS4
In der Studie zu High-Coverage Primern [4], die speziell für fungale Diversität entwickelt wurden, stellte sich heraus, dass folgende Primer höchst Pilzspezifisch sind und mehr Taxa abdecken, als die herkömmlichen Primer der selben Region:
ITS1-F_KYO1 (CTHGGTCATTTAGAGGAASTAA) - (forward)
- hohe Spezifität für Pilze, vergleichbar mit ITS1-F
- leicht reduzierten Universalität
ITS1-F_KYO2 (TAGAGGAAGTAAAAGTCGTAA) - (forward)
- höhere Abdeckung
- Vorsicht bei pflanzlicher Verunreinigung!
ITS2_KYO2 (TTYRCTRCGTTCTTCATC) - (reverse)
- höhere Abdeckung als ITS2
ITS3_KYO2 (GATGAAGAACGYAGYRAA) - (forward)
- höhere Abdeckung als ITS3
(ITS4_KYO1, ITS4_KYO2, ITS4_KYO3)
- genau so hohe Abdeckung wie ITS4
Frei aus Studie [4]:
Wie kürzlich berichtet wurde, decken mehrere klassische Primer, die häufig für die DNA-Barcodierung von Pilzen verwendet werden (z. B. ITS1, ITS1-F, ITS2 und ITS3), einen nicht unerheblichen Teil der Pilztaxa nicht ab, was potenziell zu einer taxonomischen Verzerrung der Daten führen kann. Die neu entwickelten Primer ITS1-F_KYO2, ITS2_KYO2 und ITS3_KYO2 hingegen sollten mit den Sequenzen von ca. 99 % der untersuchten pilzlichen Taxa übereinstimmen und so eine umfassende und unverzerrte DNA-Barcodierung von Ascomyceten und Basidiomyceten ermöglichen.
Grundsätzlich besteht ein Kompromiss zwischen der Spezifität für Pilze (z. B. dem Ausschluss von Pflanzentaxa) und einer unvoreingenommenen Amplifikation innerhalb des Pilzreichs. Aufgrund dieses Kompromisses sollten Barcoding-Primer-Sets entsprechend dem Zweck der ökologischen/mikrobiologischen Fragestellung ausgewählt werden. Als Ersatz für den klassischen, pilzspezifischen Primer ITS1-F wurden ITS1-F_KYO1 und ITS1-F_KYO2 für die selektive Amplifikation von Pilz-ITS-Sequenzen entwickelt.
Eine in silico PCR zeigte, dass ITS1-F_KYO1 eine hohe Spezifität für Pilze aufweist, die mit der des weit verbreiteten Primers ITS1-F vergleichbar ist. Im Gegensatz dazu könnte ITS1-F_KYO2 unter entspannten PCR-Bedingungen (z. B. niedrigen Annealing-Temperaturen) Sequenzen verschiedener Pflanzentaxa amplifizieren. Daher kann ITS1-F_KYO1 als hochspezifischer Primer für Pilze verwendet werden, allerdings mit einer leicht reduzierten Universalität.
ITS1-F_KYO2 hingegen ist ein Primer mit hoher Abdeckung, wobei das Risiko der Amplifikation pflanzlicher Sequenzen durch relativ strenge PCR-Bedingungen minimiert werden sollte.
Insbesondere war die Abdeckung von ITS4 ebenso breit wie die aller anderen Primer, einschließlich der neu entwickelten Primer. Dies deutet darauf hin, dass sowohl der klassische Primer als auch die neu entwickelten Primer für die DNA-Sequenzierung von Pilzen, die auf das 5'-Ende des ribosomalen RNA-Gens der Large Subunit abzielen, geeignet sind.
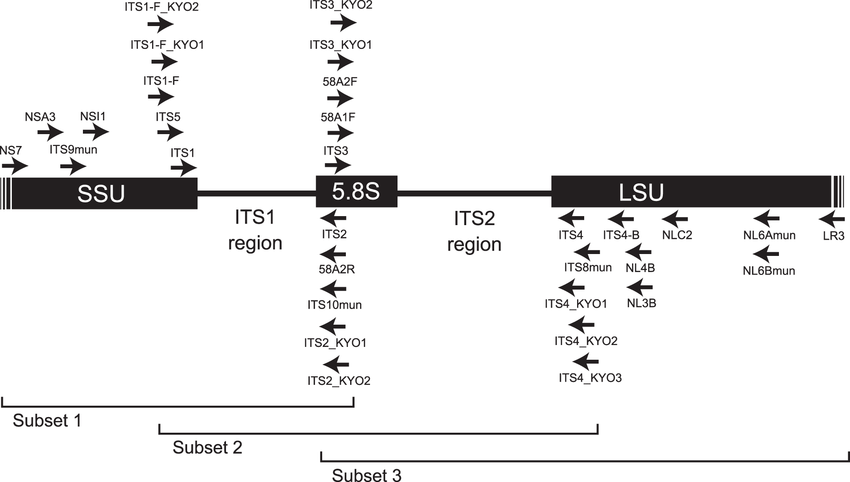
Quelle: siehe Paper [4]
¶ Tabellen von Sigrid
| Primer name | Sequence | Tm |
|---|---|---|
| ITS | ||
| Primer ITS1 | TCCGTAGGTGAACCTGCGG | 59.5° |
| Primer ITS1-F_KYO2 | TAGAGGAAGTAAAAGTCGTAA | 50.0° |
| Primer ITS1-F | CTTGGTCATTTAGAGGAAGTAA | 52.2° |
| Primer ITS2 | GCTGCGTTCTTCATCGATGC | 57.0° |
| Primer ITS3 | GCATCGATGAAGAACGCAGC | 57.0° |
| Primer ITS4 | TCCTCCGCTTATTGATATGC | 58.0° |
| Primer ITS4-B | CAGGAGACTTGTACACGGTCCAG | 59.0° |
| Primer ITS4 Cantharelllus | TCCTCCGCTTATTGATTGC | 52.6° |
| Primer ITS5 | GGAAGTAAAAGTCGTAACAAGG | 51.3° |
| LSU | ||
| Primer LR0R | ACCCGCTGAACTTAAGC | 52.4° |
| Primer LR7 | TACTACCACCAAGATCT | 45.6° |
| rpb2 | ||
| Primer RPB2-b6F | TGGGGYATGGTNTGYCCYGC | 62.7° |
| Primer RPB2-b7R | GAYTGRTTRTGRTCRGGGAAVGG | 57.9° |
| TEF | ||
| Primer EF1-983F | GCYCCYGGHCAYCGTGAYTTYAT | 61.2° |
| Primer EF1-1567R | ACHGTRCCRATACCACCSATCTT | 58.8° |
| RPB2 | |
|---|---|
| RPB2-b6F / RPB2-b7R | |
| Initial denaturation at 95 °C for 300 seconds | |
| Denaturation at 95 °C for 30s | } |
| Annealing at 55 °C for 45s | 40 cycles |
| Extension at 72 °C for 45s | } |
| Final extension at 72 °C for 420 seconds |
| LSU | |
|---|---|
| LR0R/LR7 | |
| Initial denaturation at 98 for 300 seconds | |
| Denaturation 98C 30 seconds | } |
| Annealing 47.2C for 30 seconds | 39 cycles |
| Extension 72C for 30 seconds | } |
| Final extension at 72C for 60 seconds |
| TEF1 | |
|---|---|
| EF1-983F / EF1-1567R and EF1-983F / EF1-2218R and EF1-1018F / EF1-1620R |
|
| Initial denaturation at 95C for 600 seconds | |
| Denaturation 95C 60 seconds | } |
| Annealing 62C for 60 seconds (decreasing 1 °C every 3 cycles) | 30 cycles |
| Extension 72C for 90 seconds | } |
| Final extension at 72C for 420 seconds |
¶ Geräte
- Thermocycler
- Zentrifuge
- Gelelektrophorese (siehe hier)
- Feinwaage
- Küchenwaage
- Magnetrührgerät
¶ Hilfsmittel
- 3 Mikropipetten: 1-10 µl, 2-20 µl, 20-200 µl
- feiner Permanent Marker zum Beschriften
- spitze Pinzette ohne Riffel am Ende
- Abwurfbehälter
- Tubeständer
- Erlenmeyerkolben
- Rührfisch
¶ Einkaufsliste
¶ Verbrauchsmaterialien
- 1,5 ml Eppis
- 0.2 ml PCR Tubes (oder 8-er Strips)
- Pipettenspitzen 10 µL, 100 µL, 1000 µL
- 200μl Pipettenspitzen?
¶ Reagenzien
- Destilliertes Wasser
- Natronlauge / NaOH 0,5 M
- 1M Tris (pH8.0) 1:10 verdünnt vor der Anwendung (Anleitung zur Herstellung der Stammlösung)
- TE Tris
¶ Amplifikation (PCR)
- Taq Polymerase Master Mix
(der günstigste, einfachste (Promega GoTaq)) 25 / 50 ml Flasche, auf 100 μl je Eppis verteilen (je nach dem)
Basic primer:
- ITS1-F CTTGGTCATTTAGAGGAAGTAA (forward)
- ITS1 TCCGTAGGTGAACCTGCGG (forward)
- ITS2 GCTGCGTTCTTCATCGATGC (reverse)
- ITS3 GCATCGATGAAGAACGCAGC (forward)
- ITS4 TCCTCCGCTTATTGATATGC (reverse)
- ITS4-B CAGGAGACTTGTACACGGTCCAG (reverse)
- LR0R ACCCGCTGAACTTAAGC (forward)
- LR6 CGCCAGTTCTGCTTACC (reverse)
- LR7 TACTACCACCAAGATCT (reverse)
(optional:)
- ITS1-F_KYO1 CTHGGTCATTTAGAGGAASTAA (forward)
- ITS1-F_KYO2 TAGAGGAAGTAAAAGTCGTAA (forward)
- ITS2_KYO2 TTYRCTRCGTTCTTCATC (reverse)
- ITS3_KYO2 GATGAAGAACGYAGYRAA (forward)
¶ Gelelektrophorese
- Agarose
- TBE-Puffer (TRIS-Borat-EDTA)
- Gel stain ?
- Loading dye ?
¶ Begriffe
-
Was ist Internal Transcribed Spacer?
-
Was ist TBE Buffer?
-
Was ist Mastermix?
-
Was sind dNTPs?
-
Was sind Nukleinsäuren?
-
Wofür stehen die Buchstaben der Nukleinsäuren?
¶ Stammlösung Tris-pH-8,0 (wird später 1:10 verwendet)
¶ Herstellung 50 ml
¶ Stammlösung NaOH
¶ Herstellung 30 ml
¶ Ressourcen
-
Wiki von Alan Rockefeller (Linksammlung, englisch):
https://wiki.counterculturelabs.org/wiki/DNA_sequencing -
Jerry Cooper's notes on home-based PCR for barcoding fungi:
https://www.funnz.org.nz/sites/default/files/DIY DNA PCR_2.pdf -
Sigrid's PCR protocol:
https://docs.google.com/document/d/13B9OSE_ar_vWWZnHZegr2FROnMak78qHZxEZXc1E9jk -
YouTube playlist mit DNA barcoding videos:
https://www.youtube.com/playlist?list=PLi7dEmBMB3xvyt1OY7l18BXR1VpLZcLsP -
Nanopore DNA sequencing protocol von Stephen Russell:
https://www.protocols.io/view/ont-dna-barcoding-fungal-amplicons-w-minion-amp-fl-36wgq7qykvk5 -
einsenden von Exsikkaten oder Frischmaterial möglich bei Pablo Alvarado in Spanien:
http://www.alvalab.es/index.html
¶ Papers
-
[1] Op De Beeck M, Lievens B, Busschaert P, Declerck S, Vangronsveld J, Colpaert JV. Comparison and validation of some ITS primer pairs useful for fungal metabarcoding studies. PLoS One. 2014 Jun 16;9(6):e97629. doi: 10.1371/journal.pone.0097629. PMID: 24933453; PMCID: PMC4059633.
https://pmc.ncbi.nlm.nih.gov/articles/PMC4059633/ -
[2] White TJ, Bruns TD, Lee SB, Taylor JW (1990) Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. In: Innis MA, Gelfand DH, Sninsky JJ, White TJ, editors. PCR protocols: a guide to methods and applications. United States: Academic Press. pp. 315–322.
https://www.researchgate.net/publication/223397588_White_T_J_T_D_Bruns_S_B_Lee_and_J_W_Taylor_Amplification_and_direct_sequencing_of_fungal_ribosomal_RNA_Genes_for_phylogenetics -
[3] Gardes M, Bruns TD. ITS primers with enhanced specificity for basidiomycetes--application to the identification of mycorrhizae and rusts. Mol Ecol. 1993 Apr;2(2):113-8. doi: 10.1111/j.1365-294x.1993.tb00005.x. PMID: 8180733.
https://pubmed.ncbi.nlm.nih.gov/8180733/ -
[4] Toju, Hirokazu & Tanabe, Akifumi & Yamamoto, Satoshi & Sato, Hirotoshi. (2012). High-Coverage ITS Primers for the DNA-Based Identification of Ascomycetes and Basidiomycetes in Environmental Samples. PloS one. 7. e40863. 10.1371/journal.pone.0040863.
https://www.researchgate.net/publication/229162325_High-Coverage_ITS_Primers_for_the_DNA-Based_Identification_of_Ascomycetes_and_Basidiomycetes_in_Environmental_Samples